El bioburden de los productos sanitarios
El bioburden es un término que se utiliza para describir el número de microorganismos presentes en una superficie de un objeto, dentro de él o en una porción de líquido. Desde el argot microbiológico, el término burden implica necesariamente que existe un problema respecto a la cantidad de microorganismos. Sin embargo desde su aplicación analítica, no implica necesariamente problema, sino, significa un dato cualitativo o cuantitativo para asegurar que existan un número o tipo satisfactorio o no-satisfactorio de microorganismos en una muestra (Sandle, 2013, p. 81).
Cuando el bioburden es alto para cierto objeto o material, se puede decir de forma apropiada que existe biocontaminación. Esta proposición implica también, que cuando hay algo biocontaminado, la población de microorganismos presente se distancia del bioburden típico.
Desde el punto de vista industrial, el bioburden (como calidad microbiológica) significa también un control de inocuidad importante, por lo que muchas industrias han optado incluir dentro de sus requerimientos analíticos mínimos, pruebas de bioburden, para asegurar que en su materia prima posea bioburden bajo (incluido los materiales clasificados como no estériles) y la calidad del producto de fabricación, así como la planta no se comprometa aguas abajo.
Un esquema típico de la evaluación del bioburden en un producto se muestra en la Figura 1. La lógica detrás de este esquema, supone que primero se debe conocer qué microorganismos se quieren evaluar dentro del objeto, aplicar un método y a partir de un factor de recuperación estándar validar el método. Este entonces se convierte en el método optimo para la determinación de un bioburden específico que luego se puede incluir dentro del control de rutina normal de calidad.
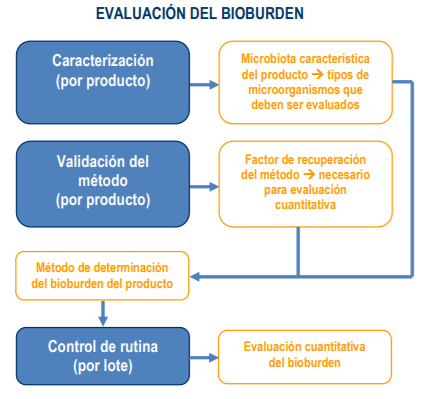
Figura 1 Diagrama de pasos analíticos para evaluación del bioburden (Eurofins, 2014)
Algunos de los ensayos típicos para determinación del bioburden se enlistan a continuación (Eurofins, 2014):
-Evaluación del bioburden del producto según ISO 11737-1. Dentro de los cuál se especifican métodos de:
- Caracterización del bioburden
- Validación del método
- Control de rutina
-Ensayo de esterilidad según ISO11737-2, USP o EP. Utilizado específicamente para:
- Determinación de endotoxinas
- Idoneidad del método según EP/USP
- LAL test según EP/USP
-Validación microbiológica del proceso de esterilización por irradiación
- Todos los métodos indicados en ISO 11137
-Evaluación de la barrera anti-microbiana de materiales de embalaje para esterilización
- Resistencia a los microorganismos según la norma alemana DIN 58953
-Ensayos microbiológicos de integridad del envase y del sistema de cierre
- Microbial challenge del envase y/o prueba de inmersión según USP o métodos internos.
-Control microbiológico de las materias primas según EP/USP, del agua de producción y de los gases.
-Control microbiológico de los ambientes de fabricación, incluyendo el muestreo.
Fuentes consultadas
Eurofins. (2014). Control Microobiológico para productos sanitarios. Barcelona.
Sandle, T. (2013). Sterility, sterilisation and sterility assurance for pharmaceuticals: technology, validation and current regulations. Oxford ; Philadelphia: Woodhead Publishing Limited.

Articulos Relacionados
Newsletter
|
|